Diversos surtos mortais causados por CRE têm sido documentados recentemente após o procedimento de endoscopia gastrintestinal (GI)
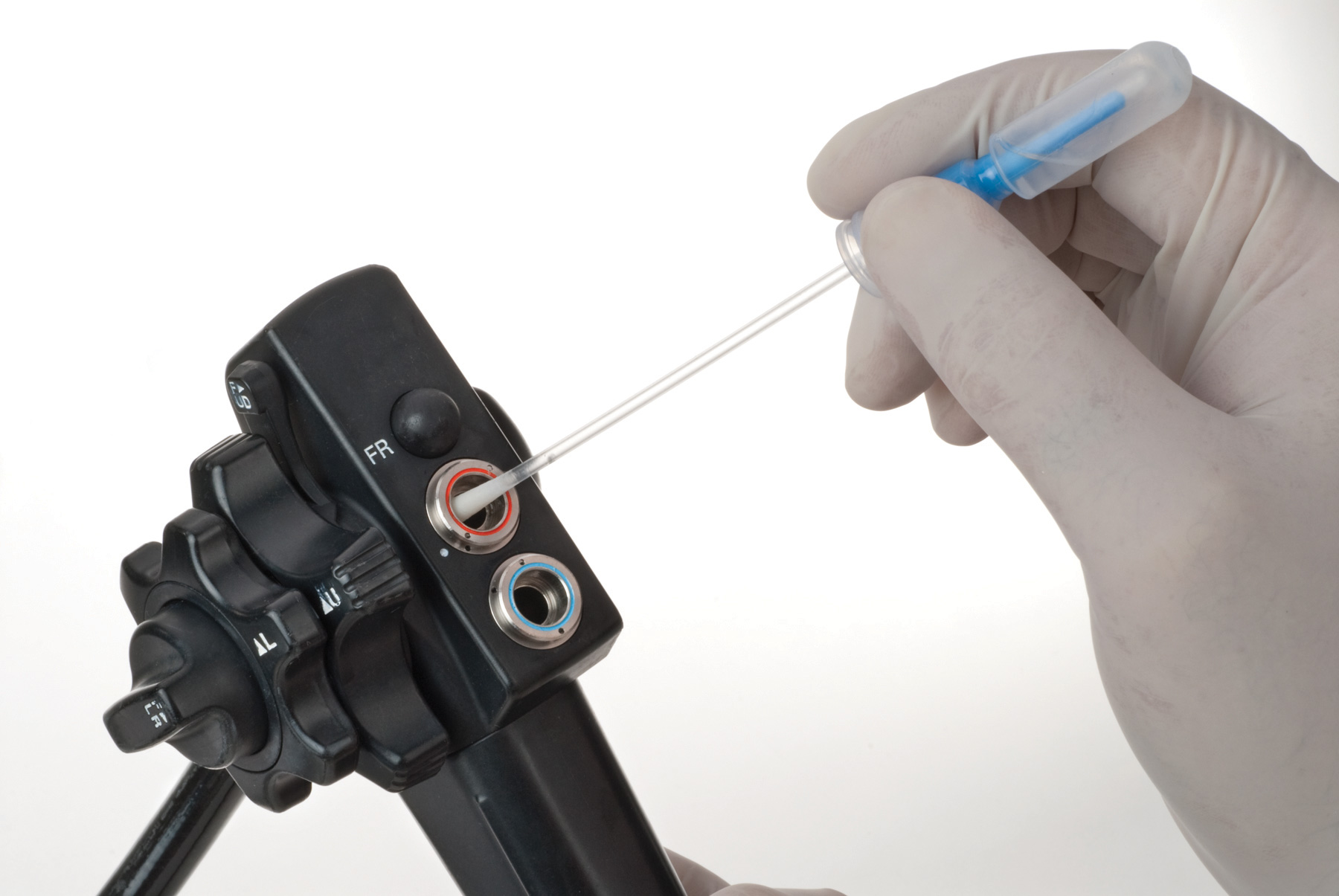
Orientações Atualizadas para a Prevenção da Transmissão de Enterobactérias Resistentes a Carbapenem (CRE) e outras Superbactérias Multidrogas Resistentes durante a Endoscopia Gastrointestinal.
Convidamos o Diretor da Planitrade, empresa representante no Brasil da The Ruhof Corporation – EUA, Sr Juarez Py de Freitas – responsável pela introdução do conceito e lançamento do primeiro detergente enzimático (Endozime) para limpeza de artigos médicos no Brasil em 1992 – para escrever sobre o artigo e discorrer a respeito do tema.
Acompanhe a matéria abaixo.
Baixe o PDF do artigo (em inglês) aqui
por Juarez Py de Freitas
Diversos surtos mortais causados por CRE têm sido documentados recentemente após o procedimento de endoscopia gastrintestinal (GI). Os profissionais da saúde associam esses surtos aos duodenoscópios ou endoscópios contaminados, que são utilizados para realizar a “CPRE” (colangiopancreatografia retrógrada endoscópica) e a “USE” (ultrassonografia endoscópica), respectivamente.
A importância de uma limpeza e desinfecção adequadas, ou “reprocessamento”, destes tipos específicos de endoscópios GI, é primordial para evitar a contaminação dos equipamentos com superbactérias. Os desenhos de duodenoscópios e endoscópios de ultrassom, no entanto, são únicos: ambos apresentam um mecanismo de elevador de fórceps, que, embora crucial para controlar e manipular a cânula, agulha ou outro acessório durante a CPRE e a USE, são difíceis de reprocessar.
A maioria dos surtos notificados de CRE ligados à um endoscópio GI contaminado ocorreu entre 2008 e início de 2015, nos EUA e na Europa. Todos os hospitais onde ocorreram o surto de CRE nos EUA utilizaram o reprocessamento automatizado (AER) e, 90% dos duodenoscópios no país são reprocessados dessa forma.
No centro da Flórida, em 2008 e 2009, duodenoscópios contaminados com CRE foram responsabilizados por um surto que afetou 70 pacientes em dois hospitais, totalizando 15 óbitos. Da mesma forma, um hospital francês informou que 16 pacientes que foram submetidos a CPRE, também entre 2008 e 2009, foram infectados com um superbactéria relacionada com a CRE.
Possivelmente associado a mais mortes do que qualquer outro surto notificado de CRE, um hospital em Seattle constatou que duodenoscópios contaminados usados entre 2012 e 2014 foram responsáveis pela infecção de 39 pacientes, 18 dos quais foram a óbito. As autoridades sanitárias concluíram que “a limpeza rotineira dos endoscópios e duodenoscópios, conforme recomendado pelo fabricante, não elimina completamente a CRE.”
Em resposta a este e outros surtos de CRE, o Food and Drug Administrtion (FDA) e o Centers for Disease Control e Prevention (CDC), entre outras agências e organizações, incluindo a Society of Gastroenterology Nurses and Associates (SGNA), publicaram uma série de recomendações para a prevenção de infecções causadas por CRE e superbactérias relacionadas após os procedimentos de CPRE e USE. O trabalho de Lawrence F. Muscarella Ph.D (LFM Healthcare Solutions, LLC) discute estas recomendações e defende mudanças, o que pode razoavelmente ser concluído para definir um novo padrão de cuidados em relação ao controle da infecção no cenário de endoscopia GI.
A maioria dos surtos reportados de CRE ou de superbactérias ligados à endoscopia GI desde 2012, tanto nos EUA como na Europa, foram associados mais significativamente à um modelo específico de duodenoscópio: o TJF-Q180V, marca Olympus. O trabalho centra-se no reprocessamento desta marca e modelo específico de duodenoscópio, embora as recomendações e orientações deste relatório possam também ser aplicadas ao reprocessamento de duodenoscópios e endoscópios de outros fabricantes, incluindo Pentax Medical, Hoya e FUJIFILM, servem também para a prevenção de surtos de superbactérias multiresistentes em outros tipos de procedimentos endoscópicos como: citoscopia, broncoscopia e colonoscopia.
As recomendações e orientações deste relatório são divididas em três seções. Na primeira são discutidas as práticas e padrões associados: reprocessamento, tempo de armazenagem e vida útil dos endoscópios e duodenoscópios, manutenção e reparo, reprocessamento de válvulas reutilizáveis, utilização e diferenciação de endoscópios para o TG inferior e superior, uso de detergentes enzimáticos que comprovem cientificamente sua capacidade de remoção de proteínas e outras matérias orgânicas dos endoscópios, além da amostragem “non-culture” (sem a realização de cultura microbiológica).
De acordo com a American Society of Gastrointestinal Endoscopy (ASGE), as técnicas de ensaio químico utilizando o ATP “podem fornecer uma ferramenta eficaz para a vigilância das etapas do reprocessamento manual do endocópio” e a capacidade dessa ferramenta de produzir resultados imediatos é uma “vantagem significativa” em comparação com as culturas microbianas padrão.
O foco da segunda seção está nas políticas e procedimentos de controle de infecção. As unidades de endoscopia GI devem fornecer aos profissionais da saúde um conjunto de diretrizes e regras que regem suas práticas de controle de infecção. Essas regras, que se baseiam nas recomendações de diretrizes publicadas (bem como as leis estaduais e federais aplicáveis), visam melhorar a qualidade e segurança, em parte, através da educação da equipe e da padronização do atendimento ao paciente. O cumprimento dessas políticas e procedimentos é essencial para a segurança do paciente.
A terceira seção discute medidas reforçadas e suplementares cuja adoção pode reduzir ainda mais o risco de transmissão de superbactérias durante a CPRE e a USE. Em agosto de 2015, o FDA publicou uma comunicação de segurança intitulada “Supplemental Measures to Enhance Duodenoscope Reprocessing” (Medidas Suplementares para Reforçar o Reprocessamento de Duodenoscópios), esta comunicação lista quatro medidas complementares que podem ajudar a reduzir o risco de transmissão de infecção associada ao uso de duodenoscópios, se realizadas juntamente com a estrita adesão às instruções de reprocessamento do fabricante dos equipamentos.
Sugere-se que as unidades endoscópicas gastrointestinais considerem implementar, pelo menos a curto prazo, uma (ou mais) destas quatro medidas suplementares para mitigar ainda mais o risco de transmissão de CRE ou de uma superbactéria relacionada durante a CPRE. Antes que uma ou mais dessas medidas possam ser implementadas, no entanto, recomenda-se a revisão completa da unidade de endoscopia GI, suas potenciais limitações, viabilidades e custos. São encorajadas comparações diretas entre essas quatro medidas para determinar quais podem ser mais seguras, mais viáveis e confiáveis, e menos dispendiosas.
O relatório do Dr. Muscarella cita as práticas recomendadas e endossadas que podem ser consideradas conclusivas para definir um novo padrão ad hoc para intensificar os cuidados no reprocessamento de duodenoscópios e endoscópios. Essas orientações devem ser periodicamente atualizadas a medida que novas informações/dados se tornem disponíveis.