Diretriz Nacional para Elaboração de Programa de Gerenciamento do Uso de Antimicrobianos em Serviços de Saúde
Gerência de Vigilância e Monitoramento em Serviços de Saúde – GVIMS
Gerência Geral de Tecnologia em Serviços de Saúde – GGTES
Brasília, 28 de dezembro de 2017
Diretriz Nacional para Elaboração de Programa de Gerenciamento do Uso de Antimicrobianos em Serviços de Saúde. GVIMS/GGTES/ANVISA
Diretor-Presidente
Jarbas Barbosa da Silva Júnior
Diretores
Alessandra Bastos Soares
Fernando Mendes Garcia Neto
Renato Alencar Porto
William Dib
Gerência Geral de Tecnologia em Serviços de Saúde – GGTES
Diogo Penha Soares
Gerência de Vigilância e Monitoramento em Serviços de Saúde – GVIMS
Magda Machado de Miranda Costa
Equipe técnica
Ana Clara Ribeiro Bello dos Santos
André Anderson Carvalho
Cleide Felícia de Mesquita Ribeiro
Fabiana Cristina de Sousa
Heiko Thereza Santana
Humberto Luiz Couto Amaral de Moura
Lilian de Souza Barros
Luana Teixeira Morelo
Mara Rúbia Santos Gonçalves
Maria Dolores Santos da Purificacao Nogueira
Elaboração
| Ana Cristina Gales | Disciplina de Infectologia, Departamento de Medicina, Escola Paulista de Medicina, Universidade Federal de São Paulo – UNIFESP/EPM |
| Carlos E. Ferreira Starling | Sociedade Brasileira de Infectologia – SBI |
| Fernando de Sá Del Fiol | Conselho Federal de Farmácia – CFF |
| Heiko Thereza Santana | Gerência de Vigilância e Monitoramento em Serviços de Saúde – GVIMS/GGTES/ANVISA |
| Henry Pablo Lopes Campos e Reis | Centro de Estudos em Atenção Farmacêutica (CEATENF)/Universidade Federal do Ceará – UFC |
| Iza Maria Fraga Lobo | Hospital Universitário -Universidade Federal de Sergipe
Hospital de Urgência de Sergipe – SES/SE |
| Julival Fagundes Ribeiro | Aliança para Uso Racional de Antimicrobianos – APUA/Brasil |
| Lauro Vieira Perdigão Neto | Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
Hospital Paulistano |
| Lucieda Araújo Martins | Coordenação Geral de Atenção Hospitalar –
Departamento de Atenção Hospitalar e de Urgência – Secretaria de Atenção à Saúde – Ministério da Saúde – GHOS/DAHU/MS |
| Lúcio Flavio Gonzaga Silva | Conselho Federal de Medicina – CFM |
| Mara Rúbia S. Gonçalves | Gerência de Vigilância e Monitoramento em Serviços de Saúde – GVIMS/GGTES/ANVISA |
| Marcelo de Oliveira Maia | Associação de Medicina Intensiva Brasileira – AMIB |
| Marcelo Silva de Oliveira | Associação Brasileira dos Profissionais em Controle de Infecções e Epidemiologia Hospitalar – ABIH |
| Maria Luísa do Nascimento Moura | Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
Hospital Samaritano de São Paulo |
| Mariana M. G. do Nascimento | Instituto para Práticas Seguras no Uso de Medicamentos – ISMP Brasil |
| Marisa de Moraes Lisboa | Gerência Geral de Medicamentos – GGMED/ANVISA |
| Maura Salaroli de Oliveira | Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo HC – FMUSP Hospital Sírio Libanês
|
| Suzie Marie Gomes | Coordenação do Centro de Gerenciamento de Informações sobre Emergências em Vigilância Sanitária – CVISA/ANVISA |
| Sylvia Lemos Hinrichsen | Universidade Federal de Pernambuco – UFPE |
Colaboração
Cleide Felícia de Mesquita Ribeiro – GVIMS/GGTES/ANVISA
Fabiana Cristina de Sousa– GVIMS/GGTES/ANVISA
Humberto Luiz Couto Amaral de Moura – GVIMS/GGTES/ANVISA
Lilian de Souza Barros – GVIMS/GGTES/ANVISA
Magda Machado de Miranda Costa – GVIMS/GGTES/ANVISA
Maria Dolores Santos da Purificação Nogueira – GVIMS/GGTES/ANVISA
APRESENTAÇÃO
A resistência microbiana aos antimicrobianos atualmente é uma das maiores preocupações globais em saúde pública, uma vez que antimicrobianos muito usados estão se tornando ineficazes, gerando uma série de consequências diretas e indiretas como, por exemplo, o prolongamento da doença, o aumento da taxa de mortalidade, a permanência prolongada no ambiente hospitalar e a ineficácia dos tratamentos preventivos que comprometem toda a população.
O combate à emergência e à propagação de bactérias resistentes aos antimicrobianos e ao desenvolvimento de novos mecanismos de resistência exige uma abordagem conjunta e articulada de vários segmentos governamentais, dos profissionais de saúde e de toda sociedade.
Nesse sentido, a Agência Nacional de Vigilância Sanitária (Anvisa) publica essa Diretriz que tem como principal finalidade orientar os profissionais dos serviços de saúde (hospitais e atenção básica) para elaboração e implementação de seus programas de gerenciamento do uso de antimicrobianos.
A publicação dessa Diretriz é uma das ações do Plano Nacional para a Prevenção e o Controle da Resistência Microbiana em Serviços de Saúde que, por sua vez, faz parte do Plano de Ação da Vigilância Sanitária em Resistência aos Antimicrobianos elaborado pela Anvisa, seguindo as recomendações da Organização Mundial de Saúde (OMS), e que demarca o papel da vigilância sanitária nos esforços brasileiros de enfrentamento à resistência aos antimicrobianos.
O presente documento foi elaborado por um grupo de trabalho formado por representantes de conselhos e associações de classe, bem como de instituições de ensino relacionadas ao tema. Além disso, por se tratar de um tema de relevância nacional, a Anvisa disponibilizou, em consulta restrita, uma minuta desse documento para receber contribuições de toda sociedade brasileira por meio de suas associações de classe e entidades representativas.
Esta diretriz não se destina a fornecer um modelo de programa de gerenciamento do uso de antimicrobianos. Ela foi desenvolvida para apresentar, de maneira abrangente, os elementos fundamentais de um programa que devem ser adaptados de acordo com a realidade, as necessidades locais, os perfis epidemiológico e microbiológico, as barreiras e os recurso do hospital ou serviços de atenção básica visando o uso ótimo de antimicrobianos nos ambientes institucionais. Além disso, traz sugestões de indicadores para medir o sucesso dessas intervenções e ainda faz recomendações da composição mínima da equipe responsável pela elaboração e implementação do programa.
A Anvisa espera com esta publicação disponibilizar aos profissionais de saúde, gestores e profissionais do Sistema Nacional de Vigilância Sanitária (SNVS), de maneira objetiva e concisa, os passos necessários para a elaboração de programas de gerenciamento do uso de antimicrobianos como uma das medidas para a luta contra a disseminação da resistência microbiana aos antimicrobianos no Brasil.
1. INTRODUÇÃO
A resistência microbiana (RM) aos antimicrobianos é uma grande ameaça à saúde pública mundial, pois gera uma série de consequências que comprometem, não apenas os pacientes, mas toda a população, como, por exemplo, o aumento da morbidade e mortalidade, o aumento do período de internação, entre outras que impõe enormes custos a todos os países. Na União Europeia, cerca de 25.000 pacientes morrem a cada ano de infecções causadas por bactérias multirresistentes e os custos associados são estimados em cerca de 1,5 bilhão de euros por ano. Já nos Estados Unidos da América, as infecções causadas por microrganismos resistentes aos antimicrobianos custam mais de 20 bilhões de dólares por ano e geram mais de 8 milhões de dias de internação hospitalar adicionais.
A resistência antimicrobiana não é um problema novo. Desde 1998, quando a Assembleia Mundial da Saúde aprovou uma resolução instando os Estados-membros a tomarem medidas contra ela, diversas estratégias de âmbito global vêm sendo publicadas pela Organização Mundial da Saúde (OMS) para o seu enfrentamento. Mas, somente em maio de 2015, na 68ª Assembleia Mundial da Saúde, foi aprovado o Plano de Ação Global para Combater a Resistência Antimicrobiana com o objetivo principal de assegurar, durante o maior tempo possível, a continuidade do tratamento bem-sucedido e a prevenção de doenças infecciosas com medicamentos efetivos, de qualidade e seguros, utilizados de forma responsável e acessíveis a todos os que deles precisam.
A OMS, em conjunto com os países-membros da Organização das Nações Unidas (ONU), incluindo o Brasil, têm estimulado a elaboração de Planos individuais de combate à resistência antimicrobiana em todo o mundo. Estes Planos devem conter ações para o combate e a contenção da resistência microbiana, entre as quais a implementação de programas para uso racional de medicamentos antimicrobianos na saúde humana e animal.
A resistência antimicrobiana é a capacidade de um microrganismo (por exemplo, uma bactéria ou um vírus) para resistir à ação de um agente antimicrobiano. É uma adaptação do microrganismo ao seu meio ambiente e resulta em uma redução ou eliminação da eficácia do agente antimicrobiano para curar ou prevenir a infecção causada por este microrganismo. As bactérias, por exemplo, podem ser naturalmente resistentes a certos antibióticos (resistência intrínseca ou inerente), mas um problema mais preocupante é quando algumas bactérias que são normalmente suscetíveis a antibióticos tornam-se resistentes como resultado da adaptação por meio de mudanças genéticas (resistência adquirida).
Embora a resistência microbiana seja um fenômeno natural, sua propagação está diretamente relacionada a diversos fatores, como uso indevido de antimicrobianos, programas de controle de infecção e de gerenciamento da terapia antimicrobiana inadequados ou inexistentes, medicamentos de má qualidade, vigilância inadequada e regulamentação insuficiente sobre o uso dessas substâncias.
As infecções causadas por bactérias resistentes podem exigir mais cuidados, bem como antimicrobianos alternativos e mais caros, que também podem ter efeitos colaterais mais graves. Uma vez estabelecida em uma pessoa, bactérias resistentes aos antimicrobianos podem ser transmitidas para outra pessoa. O alto consumo desses medicamentos em uma população (hospital ou comunidade) favorece fortemente a propagação dessas bactérias4.
Os antimicrobianos são a segunda classe de medicamentos mais utilizada em hospitais e responsável por 20 a 50% das despesas hospitalares com medicamentos, além de serem também prescritos em larga escala em nível ambulatorial. Este amplo uso pode afetar significativamente tanto a microbiota do indivíduo quanto a do ambiente hospitalar.
Assim, o controle e a prevenção da disseminação da resistência microbiana aos antimicrobianos pelos serviços de saúde é imperativo nos dias atuais. Nesse aspecto, uma das abordagens para combater esse problema é o desenvolvimento de programas de gerenciamento de uso de antimicrobianos. A implementação desses programas, além de visar aumentar a segurança do paciente e garantir bons resultados clínicos do uso de antimicrobianos, minimizando suas consequências não intencionais, tais como efeitos adversos e resistência microbiana, podem resultar também na redução de custos para os serviços de saúde.
Dessa forma, a Gerência de Vigilância e Monitoramento em Serviços de Saúde (GVIMS), da Gerência Geral de Tecnologia em Serviços de Saúde (GGTES), da Agência Nacional de Vigilância Sanitária (Anvisa), alinhada com os objetivos do Plano de Ação Global da OMS e com o Programa Nacional de Prevenção e Controle de Infecções Relacionadas à Assistência à Saúde (PNPCIRAS) convidou um Grupo de Especialistas brasileiros para elaborar um documento que pudesse orientar os profissionais que atuam nos serviços de saúde na elaboração e execução de Programas de Gerenciamento do Uso de Antimicrobianos nos serviços de saúde do país. Este documento, intitulado Diretriz Nacional para Elaboração de Programa de Gerenciamento do Uso de Antimicrobianos em Serviços de Saúde, é o resultado do esforço desses colaboradores.
2. OBJETIVO
Orientar os profissionais de saúde na elaboração e implementação de programas de gerenciamento do uso de antimicrobianos nos serviços de saúde.
3.1 AÇÕES PARA ELABORAÇÃO E IMPLEMENTAÇÃO DO PROGRAMA DE GERENCIAMENTO DE USO DE ANTIMICROBIANOS EM HOSPITAIS
Os hospitais são serviços de saúde que podem apresentar alta prevalência de microrganismos multirresistentes, o que, em geral, leva ao uso de antimicrobianos de amplo espectro e alto custo, tornando imprescindível a implementação de um programa de gerenciamento do uso desses medicamentos de forma a minimizar os danos decorrentes da resistência microbiana e melhorar os desfechos clínicos.
A obrigatoriedade de elaboração e implementação de um programa para uso racional de antimicrobianos nos serviços de saúde pelas Comissões de Controle de Infecção Hospitalar (CCIH) foi estabelecida na Portaria GM/MS nº 2616, de 12/05/1998. Já a RDC Anvisa nº 07/2010, que dispõe sobre os requisitos mínimos para funcionamento das Unidades de Terapia Intensiva (UTI), em seu Art. 45 determina que a equipe desta Unidade proceda ao uso racional de antimicrobianos, estabelecendo normas e rotinas de forma interdisciplinar e em conjunto com a CCIH, Farmácia Hospitalar e Laboratório de Microbiologia.
Constituem elementos essenciais para a criação, implantação e execução desse Programa nos hospitais:
Apoio da alta direção do hospital;
Definição de responsabilidades de todos os profissionais envolvidos;
Educação;
Desenvolvimento de ações para melhorar a prescrição de antimicrobianos;
Monitoramento do programa e
Divulgação de resultados.
3.1.1 Apoio da alta direção
O êxito no desenvolvimento e na implementação do Programa de Gerenciamento de Uso de Antimicrobianos dentro do hospital depende da dedicação de recursos humanos, financeiros e tecnológicos, do apoio e colaboração das lideranças médicas bem como da administração hospitalar15. A relação custo-efetividade dessas medidas já foi demonstrada em vários estudos, considerando-se a economia com o uso de antimicrobianos e com os gastos indiretos, tais como morbidade e menor tempo de internação dos pacientes.
3.1.2 Definição de responsabilidades
A direção do hospital deve nomear um time gestor responsável por definir as políticas e normativas, bem como as diretrizes gerais, monitoramento contínuo, propostas de melhoria e retroalimentação dos resultados (feedback) do Programa de Gerenciamento de Uso dos Antimicrobianos.
É recomendável que o time gestor seja interdisciplinar e composto, minimamente, por um representante da (o):
Alta gestão institucional;
CCIH;
Equipe médica;
Equipe de enfermagem;
Farmácia clínica;
Laboratório de microbiologia;
Tecnologia da informação e
Coordenações de setores estratégicos para o gerenciamento do uso de antimicrobianos como, por exemplo, unidades clínicas e assistências (UTI, Centro Cirúrgico e obstétrico, clínica médica, emergência, Centro de oncologia, etc.) e as unidades de apoio (farmácia, laboratório de análises clínicas, núcleo de qualidade, gerenciamento de risco ou segurança do paciente, entre outros).
Os representantes da CCIH e da equipe médica que compõem o time gestor devem, preferencialmente, ser infectologistas ou, na ausência desse profissional, médicos com expertise em doenças infecciosas. No caso do farmacêutico clínico ou outro profissional de saúde, o ideal é que o mesmo possua expertise em doenças infecciosas e uso de antimicrobianos.
Deve ser definido um líder do time gestor responsável por reportar à direção do serviço de saúde as necessidades e resultados relacionados ao Programa.
O líder do time gestor deve coordenar as ações administrativas e gerais do Programa. Sua liderança pode aumentar a aceitação e o cumprimento do Programa nas diferentes unidades do hospital. Este deverá participar de todas as instâncias, definições e monitoramento de estratégias e intervenções. Em particular, deve procurar estabelecer um consenso geral a respeito da padronização de processos e mecanismos de avaliação e controle sistemáticos e periódicos entre os diferentes setores do hospital.
O monitoramento das estratégias e intervenções deve ser feito por meio de uma agenda de reuniões, previamente programadas, com todo o time de gestão para discussão das metas pactuadas, analisando o alcance ou não das mesmas e o redirecionamento do Programa, quando necessário.
Sugere-se que o líder do time gestor seja o representante da alta gestão do serviço de saúde, com governabilidade para garantir a sustentabilidade das ações clínicas, técnicas e administrativas do Programa. Visando seu maior engajamento com os resultados a serem alcançados, é recomendável que a efetividade do Programa faça parte de suas metas de desempenho individuais.
Além do time gestor, é necessário definir também o time operacional que é responsável pela elaboração, execução e monitoramento das ações do Programa de Gerenciamento.
O time operacional deve ser formado, minimamente, pelos seguintes componentes do time gestor: infectologista ou médico com expertise em doenças infecciosas, farmacêutico clínico preferencialmente com expertise em doenças infecciosas e uso de antimicrobianos, enfermeiro da CCIH e microbiologista clínico.
Para coordenar as atividades do time operacional é necessário definir um líder operacional que, preferencialmente, deve ser um infectologista / médico com expertise em doenças infecciosas ou um farmacêutico clínico com conhecimento em doenças infecciosas. Esse coordenador deve ter o seu trabalho alinhado com a CCIH e com a Comissão de Farmácia e Terapêutica (CFT) do hospital.
Além da especialidade do líder operacional, o sucesso do Programa dependerá do seu conhecimento no manejo racional dos antimicrobianos, da sua capacidade de liderança e do seu compromisso com o Programa.
O líder operacional deve participar ativamente de outros grupos envolvidos com a melhoria do uso dos antimicrobianos (exemplo: profilaxia cirúrgica; diagnóstico e tratamento de sepse, CFT, etc.)
Todos os setores do hospital têm papel importante na execução do Programa, desta forma, devem haver lideranças técnicas que atuem como suporte na operacionalização das ações estratégicas do Programa. Para tanto, é recomendado que essas ações façam parte da descrição das atividades desses profissionais nos setores, os quais devem contar com tempo e recursos para sua execução.
A efetividade das ações do Programa depende da atuação conjunta de diferentes setores hospitalares que exercem funções específicas dirigidas para esse fim. Assim, o setor de microbiologia deve reportar a identificação e o perfil de sensibilidade aos antimicrobianos; a CCIH deve fornecer dados relacionados à etiologia das infecções relacionadas à assistência à saúde (IRAS) e vigilância de microrganismos multirresistentes; a enfermagem e a farmácia devem revisar os medicamentos prescritos; a equipe de tecnologia da informação deve oferecer recursos que integrem sistemas para qualificar e facilitar a prescrição, a dispensação e a distribuição do medicamento no serviço de saúde, além da análise dos resultados. A CCIH e a CFT são importantes para a padronização e a avaliação da qualidade dos antimicrobianos a serem adquiridos, incluindo a qualificação dos fornecedores.
3.1.3 Educação
A educação é um componente essencial para o sucesso do Programa de Gerenciamento do Uso de Antimicrobianos, que transpassa todas ou quase todas as suas estratégias. Um aspecto importante é o treinamento continuado para toda a instituição sobre o Programa e sobre as ações estratégias para setores específicos envolvidos. É importante estabelecer prioridades educacionais de acordo com as principais dificuldades detectadas e os problemas mais prevalentes.
3.1.3.1 Educação dos profissionais de saúde
A educação profissional permanente visa aumentar a conscientização sobre o uso dos antimicrobianos, por meio de aulas, discussões in loco, visitas interdisciplinares à beira do leito, seminários e treinamentos adaptados às equipes as quais se dirigem. Essas capacitações devem abordar tópicos sobre antimicrobianos como farmacologia e farmacoterapia, boas práticas de preparo e administração, epidemiologia das infecções, medidas de prevenção e controle de infecções, mecanismos de resistência dos microrganismos aos antimicrobianos, reações adversas, interações medicamentosas, entre outros.
É desejável enfatizar os aspectos básicos do uso de antimicrobianos nos treinamentos realizados na admissão de novos profissionais do hospital.
A educação sobre causas e tendências da resistência aos antimicrobianos e orientação sobre abordagens para promover as boas práticas de prescrição são fundamentais para a efetividade do Programa. Independentemente da disciplina, as oportunidades de treinamento contínuo devem estar disponíveis para médicos, farmacêuticos, enfermeiros e demais profissionais de saúde da instituição.
Por outro lado, existem também várias ferramentas de educação à distância, cujo uso deve ser estimulado pelo time operacional do Programa. A vantagem desta metodologia e de outras instâncias de educação virtual é que evita a duplicação de esforços necessários para a execução de novos cursos presenciais e permite que os profissionais de saúde realizem os treinamentos em seus horários disponíveis.
3.1.3.2 Educação dos Pacientes e Acompanhantes/Cuidadores
No processo educacional é fundamental o envolvimento dos pacientes e de todos que o cercam, principalmente dos familiares ou cuidadores, visando a conscientização para o uso correto dos antimicrobianos.
O profissional de saúde deve orientar os pacientes para o uso correto dos antimicrobianos. O paciente/familiar/cuidador sempre deve ser orientado, com linguagem acessível, em relação à indicação do antimicrobiano, quanto a via de administração, a posologia, o tempo de tratamento e todos os cuidados que devem ser tomados durante o tratamento.
É importante que o profissional verifique com o paciente/familiar/cuidador se eles entenderam toda a explicação, para que as dúvidas que ainda restaram possam ser sanadas.
3.1.4 Desenvolvimento de ações para melhorar a prescrição de antimicrobianos
A utilização correta de antimicrobiano envolve a avaliação criteriosa sobre sua necessidade de uso, a escolha de um fármaco eficaz, seguro, com custo equilibrado e que seja administrado por tempo, dose e intervalos posológicos apropriados.
As ações voltadas para a melhoria do uso de antimicrobianos vão desde abordagens educativas até medidas restritivas, entre as quais podemos citar:
Utilização de protocolos clínicos para as principais síndromes clínicas;
Adoção das boas práticas de prescrição, como documentação de dose, duração e indicação do antimicrobiano;
Auditoria prospectiva de prescrição com intervenção e divulgação dos dados;
Readequação da terapia, conforme resultados microbiológicos;
Análise técnica das prescrições pela farmácia;
Restrição com uso de formulário terapêutico e pré-autorização de antimicrobianos.
3.1.4.1 Elaboração de protocolos clínicos
A elaboração de protocolos clínicos com base em evidências científicas e em práticas de consensos é de fundamental importância para orientar as ações dos profissionais de saúde, tanto de técnicos quanto de gestores. Foi demonstrado que a adoção de protocolos de uso de antimicrobianos é efetiva na promoção do uso correto desses fármacos e, por isso, tal estratégia tem sido adotada por vários países.
Os serviços de saúde devem elaborar ou adaptar seus próprios protocolos, de acordo com as características clínicas e com os perfis epidemiológico e microbiológico locais. Para isso, é importante analisar se existem guias regionais ou nacionais para adaptá-los às condições epidemiológicas (prevalência de principais patógenos e seus respectivos antimicrobianos), recursos de diagnóstico e arsenais terapêuticos institucionais.
É necessário que os protocolos sejam objetivos, para que na prática clínica seu uso seja simples e rápido, e que incorporem o perfil microbiológico do setor no qual serão usados, já que a epidemiologia pode variar entre setores de uma mesma instituição. Além disso, devem ser atualizados periodicamente.
A adoção de protocolos permite reduzir diferenças de condutas entre os profissionais e melhorar a avaliação de processos e resultados, aumentando assim a qualidade e a segurança da assistência. Além disso, ao posicionar as drogas com maior espectro, toxicidade ou custos em indicações específicas, atuam, de alguma forma, como diretrizes restritivas.
A elaboração dos protocolos deve ser realizada por uma equipe multiprofissional e contemplar os seguintes tópicos:
Definição da síndrome clínica e dos objetivos;
Realização de pesquisa bibliográfica;
Análise do perfil de sensibilidade microbiológico da instituição;
Estabelecimento da periodicidade de revisão e de atualização.
É fundamental que os prescritores da instituição de saúde façam parte da equipe multiprofissional responsável pela elaboração dos protocolos. O simples fato de desenvolver e divulgar protocolos sem uma discussão prévia com os prescritores geralmente não é uma intervenção efetiva.
Os protocolos hospitalares devem estabelecer o regime antimicrobiano de escolha, considerando a dose e a duração do tratamento para, no mínimo, antibioticoprofilaxia cirúrgica, realização de procedimentos invasivos e para as seguintes infecções, de acordo com a característica do serviço de saúde:
– Infecções comunitárias:
Endocardite
Infecção de pele/partes moles
Infecção do trato urinário baixo
Infecção intra-abdominal
Infecções do trato respiratório alto
Infecções intestinais
Infecções osteo-articulares
Meningite
Pielonefrite
Pneumonia
Sepse
– Infecções Relacionadas à Assistência à Saúde (IRAS)
Infecção da corrente sanguínea
Infecção de sítio cirúrgico
Infecção do trato urinário
Pneumonia /traqueobronquite
Sepse
Ventriculites
A divulgação desses protocolos e o treinamento de todos os profissionais da instituição na sua implementação, a interação entre profissionais executores e gestores, o estabelecimento de metas, bem como o monitoramento periódico de sua adoção são fundamentais para o êxito do Programa.
3.1.4.2 Auditoria da prescrição de antimicrobianos
A auditoria de antimicrobianos consiste em revisar sistematicamente, no momento da sua prescrição ou retrospectivamente, sua indicação, posologia e duração do tratamento.
Preferencialmente, para uma maior redução do uso inadequado de antimicrobianos, a auditoria deve ser feita por um infectologista, um farmacêutico clínico ou outro profissional com treinamento ou formação em doenças infecciosas ou no uso desses medicamentos.
A. Auditoria retrospectiva
A auditoria retrospectiva pode ser realizada por meio da avaliação dos formulários de solicitação de antimicrobianos preenchidos pelo prescritor, em formato impresso ou eletrônico, no qual conste, entre outras informações, a justificativa para o seu uso. Outra possibilidade consiste na obtenção de relatórios de antimicrobianos prescritos, que podem ser disponibilizados pela farmácia ou obtidos por sistemas eletrônicos.
É recomendável que a auditoria retrospectiva seja realizada após 48 horas da prescrição, quando já há melhor definição do quadro clínico e disponibilidade de resultados de testes diagnósticos, podendo ser feita a adequação com base no resultado de culturas ou a suspensão do tratamento, quando o diagnóstico de infecção bacteriana tiver sido descartado, de acordo com a evolução clínica e os resultados de exames laboratoriais.
É importante que após a realização da auditoria retrospectiva, os médicos sejam informados sobre a conformidade das suas prescrições de antimicrobianos, por meio de contato direto (pessoalmente) ou indireto (por telefone, por e-mail, mensagens, etc.).
A realização da auditoria requer tempo e dedicação de recursos humanos especializados. Frente à falta de recursos adequados pode-se priorizar a avaliação da prescrição de antimicrobianos de maior espectro, de maior custo ou reservados para infecções por microrganismos multirresistentes, como, por exemplo, piperacilina/tazobactam, carbapenêmicos, polimixinas, tigeciclina, linezolida, vancomicina, teicoplanina, daptomicina, cefalosporinas de terceira e quarta geração, entre outros.
Uma estratégia fundamental que pode ser adotada é a auditoria de todos os pacientes que estejam recebendo antimicrobianos por mais de sete dias, tempo suficiente para tratar a maior parte das infecções.
É importante garantir que toda prescrição de antimicrobianos siga as recomendações de boas práticas de prescrição de antimicrobianos (Anexo I) e que a indicação, a dose, a duração e o tempo do uso do antimicrobiano estejam facilmente identificáveis. Tornar tais informações acessíveis facilita o processo de auditoria da prescrição, além de possibilitar que os medicamentos sejam modificados conforme a necessidade ou descontinuados em tempo hábil.
B. Auditoria prospectiva interdisciplinar
Também chamada de revisão pós-prescrição, é desenvolvida em geral por meio de visitas programadas, periódicas e conjuntas entre membros do time operacional e médicos assistenciais e residentes da unidade hospitalar. Essas visitas incluem a revisão e a discussão de todos antimicrobianos em uso na unidade ou apenas dos estratégicos ou os de reserva.
Para que essa auditoria seja efetiva, é fundamental que o modelo interdisciplinar de decisão compartilhada seja difundido e que os papeis éticos e técnicos de todos os envolvidos sejam claramente entendido por todos os profissionais da instituição.
3.1.4.3 Medidas Restritivas
A restrição antimicrobiana, realizada por meio da utilização de formulário de restrição ou exigência de pré-autorização, é o método mais eficaz de controle do uso de antimicrobianos.
Em situações especiais, como por exemplo, antimicrobiano reservado para tratamento de bactérias multirresistentes, pode-se optar por um sistema de pré-autorização com maior controle da prescrição, onde só é possível a liberação desse antimicrobiano pela farmácia após contato do médico prescritor com os responsáveis pelo Programa dentro do serviço de saúde. É importante garantir que tal medida não atrase o tratamento de pacientes independente do dia e do horário, por exemplo em caso de prescrições à noite, finais de semana ou feriado.
Cada serviço de saúde deve definir sua relação dos antimicrobianos com restrição ou com necessidade de pré-autorização, considerando, entre outros fatores, seu perfil de sensibilidade microbiológico.
As principais vantagens das medidas restritivas são: controle mais direto sobre o uso de antimicrobianos; oportunidades para educação individual; prevenção para o uso desnecessário de antimicrobianos; redução imediata e substancial no uso desses medicamentos e nos custos associados.
Entre as desvantagens, podemos citar: requer alta disponibilidade do líder operacional; pode atrasar a administração da prescrição enquanto a aprovação é obtida, com potencial de resultados adversos para o paciente; dificuldade de aceitação da intervenção pelos prescritores, principalmente na fase inicial da implantação do Programa; percepção de “perda de autonomia” do prescritor devido à pré-autorização; possível aumento do uso de agentes antimicrobianos alternativos e consequentemente da sua resistência.
A pré-autorização e a auditoria prospectiva com retroalimentação dos resultados para os prescritores melhoram o uso de antimicrobianos e são componentes centrais de qualquer programa de gerenciamento do uso desses medicamentos. Assim, o Programa deve conter uma dessas estratégias ou uma combinação de ambas, considerando a disponibilidade de recursos específicos do serviço de saúde para uma implementação consistente. Cabe reforçar que a adoção de uma dessas estratégias é essencial para a implementação exitosa do Programa.
3.1.4.4 Ações complementares
Além das ações estratégias descritas acima (elaboração de protocolos, auditoria com retroalimentação dos resultados e medidas restritivas) cuja implementação é altamente recomendável, existem ações complementares que melhoram muito o gerenciamento do uso de antimicrobianos da instituição. A seguir apresentamos alguns pontos importantes de algumas dessas ações.
A. Revisão pelos prescritores das prescrições em 48-72 horas
Esta estratégia envolve os médicos prescritores de todas as unidades de hospitalização, fortalecendo o conceito de que gerenciar o uso de antimicrobianos não é da exclusiva responsabilidade do time do Programa.
Os prescritores devem ser encorajados a realizar a revisão da prescrição após dois ou três dias de tratamento, quando há mais informações clínicas e microbiológicas disponíveis. É importante que esses profissionais incluam formalmente a seguinte informação no registro médico:
Esquema antimicrobiano em progresso (nome do medicamento, dose, via, posologia, dias decorridos e duração provável);
Diagnóstico atualizado;
Resultados laboratoriais;
Avaliação das possibilidades de redução do espectro (descalonamento), de acordo com os achados microbiológicos; e
Possibilidade de passagem do antimicrobiano para via oral.
A inclusão de uma lista de verificação no registro médico pode aumentar significativamente a adesão a esta estratégia. Tal como acontece com todas as estratégias, a educação para prescritores é crítica. A combinação da revisão por prescritores alinhada com a auditoria prospectiva interdisciplinar, proporciona mais treinamento e engajamento desses profissionais com o Programa.
B. Intervenções guiadas pela farmácia
A farmácia deve atuar de forma complementar nas ações de gerenciamento do uso dos antimicrobianos. Nesse sentido, entre as ações que a farmácia pode executar, podemos exemplificar:
Sugestão de terapia sequencial, ou seja, sugerir a conversão da via intravenosa para oral em situações apropriadas e para antimicrobianos com boa absorção (por exemplo, fluoroquinolonas, trimetoprim-sulfametoxazol, linezolida, etc.);
Ajustes da dose em casos de disfunção orgânica (por exemplo, ajuste em função renal alterada);
Otimização da dose, levando em consideração as características do paciente (por exemplo, idade, peso, função renal), o microrganismo causador, o sítio da infecção e as características farmacocinéticas e farmacodinâmicas do agente antimicrobiano, incluindo ajustes de dose com base no monitoramento de terapêutico, por exemplo vancomicina;
Alertas automáticos em situações em que a terapia está desnecessariamente duplicada, por exemplo, uso simultâneo de fármacos com espectros sobrepostos;
Alertas ou até mesmo suspensão automática, de acordo com o tempo de uso, especialmente em antibióticos administrados para profilaxia cirúrgica;
Detecção e prevenção de interações medicamentosas relacionadas a antimicrobianos.
3.1.4.5 Suporte da tecnologia de informação (TI)
O uso da tecnologia de informação (TI) nos hospitais está crescendo, embora o grau de desenvolvimento varie significativamente entre instituições, cidades, regiões e países. Em relação ao seu uso no Programa, a contribuição desta tecnologia pode variar desde a disponibilização de ferramentas básicas (por exemplo, banco de dados, monitorização microbiológica, etc.) até a utilização de ferramentas mais sofisticadas que fornecem suporte para decisão clínica e de gestão como, por exemplo, as avaliações farmacoeconômicas.
A TI é fundamental para a integração e a melhoria dos processos desenhados dentro do Programa, pois a maioria das ações requer informações rápidas e precisas, que podem ser fornecidas por uma boa ferramenta informatizada.
Em resumo, o uso de TI no contexto do Programa pode ser progressivo em cada hospital. Minimamente, são necessários bancos de dados desenvolvidos em pacotes computacionais comuns (como por exemplo Excel®) para ajudar na análise dos parâmetros do Programa, progredindo, de acordo com a evolução do mesmo e os recursos disponíveis, para níveis mais altos de tecnologia, como por exemplo, a utilização de um software desenhado especificamente para este fim.
3.1.5 Monitoramento do Programa
O monitoramento das ações estratégicas e dos resultados relacionados ao Programa tem o objetivo de avaliar o impacto das intervenções, identificar potenciais áreas de melhoria e promover o retorno das informações para todos os profissionais envolvidos.
Os principais indicadores utilizados para o monitoramento dos programas de gerenciamento do uso de antimicrobianos podem ser divididos em duas categorias:
Indicadores ou medidas de processo: qualidade na utilização de antimicrobianos;
Indicadores ou medidas de desfecho/resultado: resistência microbiana, taxas de infecção por Clostridium difficile, resultados clínicos (extensão da permanência, taxa de readmissão e mortalidade) e redução de custos.
Os indicadores do Programa devem ser definidos de forma que possam apontar se as atividades propostas estão sendo bem executadas (indicadores de processo ou desempenho), ou se os objetivos propostos foram alcançados (indicadores de resultado e de impacto). A seguir, apresentamos sugestões de indicadores que podem ser utilizados, de acordo com as atividades e objetivos do Programa, sendo que outros indicadores podem ser monitorados, conforme as características das unidades e dos serviços de saúde.
3.1.5.1 Indicadores de Processo para Avaliação do Consumo e Uso de Antimicrobianos
Várias medidas podem ser utilizadas para mensurar e avaliar o consumo e o uso de antimicrobianos em hospitais. A medida de consumo mais amplamente utilizada é a Dose Diária Definida (Defined Daily Dose – DDD) preconizada pela OMS e IDSA. No entanto, novas medidas vêm sendo adotadas para o aprimoramento das análises como “Dias de Terapia” (Days of therapy – DOT) e “Duração de Terapia” (Lenght of therapy – LOT), que podem ser ferramentas bastante úteis para o monitoramento e a análise do uso de antimicrobianos, mostrando-se sob certos aspectos, melhores e com relevância clínica maior que a DDD32.
Os indicadores para avalição de consumo devem ser calculados mensalmente, de forma global para todos os antimicrobianos usados no hospital ou por setores específicos. Podem ainda ser estratificados por cada grupo de antimicrobianos ou para cada um destes, individualmente, de acordo com a realidade do serviço de saúde.
A tendência de evolução temporal do uso de antimicrobianos pode ser avaliada em gráficos de tendência onde são mostradas as taxas mensais ao longo do tempo de monitoramento.
A. Medida do Consumo de Antimicrobiano
Medidas de consumo refletem um agregado ou quantidade média de antimicrobianos, expressos em gramas, que estão sendo utilizados em nível de paciente, de um serviço, de uma unidade ou do hospital.
Dose Diária Definida (DDD) é a dose média diária de manutenção do antimicrobiano, expressa em gramas, habitualmente usada por um adulto de 70 Kg, para a principal indicação terapêutica daquele medicamento. Esta é a unidade utilizada pelo Conselho Nórdico sobre Medicamentos, pioneiro nos estudos de utilização de medicamentos e é a unidade recomendada pelo Grupo de Estudos de Utilização de Medicamentos da OMS.
É importante destacar que a DDD é uma unidade de medida e não reflete necessariamente a dose diária recomendada ou prescrita. Os dados de consumo de antimicrobianos apresentados em DDD apenas dão uma estimativa aproximada do consumo e não uma imagem exata do uso real, mas permite que se avalie as tendências no consumo dessas drogas e faça comparações entre grupos populacionais.
A OMS recomenda que, para a realização de estudos de consumo de antimicrobianos que sejam comparativos entre diferentes unidades hospitalares, em âmbito internacional ou entre períodos em uma mesma localidade, os dados de consumo sejam levantados de forma padronizada. Nesse sentido, ela preconiza o uso da DDD como unidade padronizada para a medida do consumo de medicamentos.
Uma vantagem do uso da DDD em hospitais é a relativa facilidade na obtenção deste dado, em especial quando o sistema de prescrição ou dispensação é informatizado. Assim, a DDD tem sido amplamente utilizada como uma medida global para avaliar programas de gerenciamento de uso de antimicrobianos em hospitais.
Fórmula de cálculo da DDD:
DDD = ____A / B____ x 1000
P
A= Total do antimicrobiano consumido em gramas (g), no período de tempo considerado
B= Dose diária padrão do antimicrobiano calculado em gramas para adulto de 70kg, sem insuficiência renal (definido pela OMS)
P= Pacientes-dia, no período de tempo considerado
As DDD para os antimicrobianos estabelecidas pela OMS são revisadas regularmente e podem ser obtidas em https://www.whocc.no/atc_ddd_index/
B. Medida de uso de antimicrobianos (DOT e LOT)
As medidas de uso refletem um agregado ou quantidade média de antimicrobianos expressos em dias de utilização, sendo utilizados em nível do paciente, de um serviço, unidade ou hospital.
- Dias de Terapia – (“Days of Therapy“- DOT)
Dias de Terapia (DOT) vem sendo apontada recentemente como a medida mais apropriada para avaliação do impacto de programas de gerenciamento de uso de antimicrobianos35, embora, a maioria dos estudos publicados que descreveram reduções significantes no uso de antimicrobianos, empregaram a DDD como medida padrão. O número de dias em que um paciente recebe um agente antimicrobiano (independentemente da dose) equivale ao DOT. Qualquer dose de um antimicrobiano recebida durante um período de 24 horas representa 1 DOT. Por exemplo, num tratamento com esquema combinado de três antimicrobianos por 10 dias, seriam contados 30 DOTs, 10 DOTs para cada antimicrobiano. Para a mesma indicação clínica, se adotada a monoterapia (apenas 1 antimicrobiano), a soma seria de 10 DOTs.
Fórmula do DOT:
Número total (somatória) de dias de uso de cada antimicrobiano X 1000
Total de pacientes-dia
A avaliação do DOT oferece maior precisão na relação entre o tratamento recebido quando comparado a DDD. O conceito de “dias de exposição” vem surgindo como mais apropriado que o termo “dias de terapia” para expressar situações especiais em que são usados antimicrobianos de meia-vida longa, especialmente na insuficiência renal.
Duração da Terapia (“Lenght of Therapy” – LOT)
O número de dias em que o paciente recebe agentes antimicrobianos sistêmicos, independentemente do número de fármacos, corresponde à LOT. Portanto, a LOT será menor ou igual ao DOT já que cada antimicrobiano recebido comporta a sua própria DOT.
Fórmula da LOT:
Número total (somatória) de dias de uso de todos os antimicrobianos juntos X 1000
Total de pacientes-dia
Ao contrário do DOT, a LOT não pode ser usada para comparar o uso de drogas específicas, mas fornece uma avaliação mais precisa da duração da terapia antibacteriana.
Razão DOT/LOT
A razão DOT / LOT, calculada pela simples divisão do valor do DOT pelo valor da LOT, pode ser útil para avaliar a frequência de combinação de terapia antimicrobiana versus a monoterapia – quando a razão é igual a 1 identifica-se a monoterapia, quando maior que 1, identifica-se que uma combinação terapêutica foi utilizada.
| RAZÃO DOT/LOT | INTERPRETAÇÃO |
| IGUAL A 1 | MONOTERAPIA |
| MAIOR QUE 1 | COMBINAÇÃO DE ANTIMICROBIANOS |
Tanto o DOT quanto a LOT são medidas de densidade de incidência expressas por 1000 pacientes-dia (mais amplamente usada) ou por 100 pacientes-dia. Pode ainda ser calculada por 100 admissões de forma que possibilite a comparação entre hospitais ou serviços de diferentes tamanhos.
C. Diferenças, indicações e limitações para o uso da DDD, DOT e LOT
A DDD foi criada para medir o consumo de antimicrobianos em programas de gerenciamento do uso de antimicrobianos e existem diferentes razões para que não seja usada especificamente para medir o impacto do programa no uso destes medicamentos. Sua incapacidade em mostrar o número de pacientes de fato expostos aos fármacos constitui-se numa limitação importante. Outra limitação fundamental ao uso da DDD é a população pediátrica. Os números ficam não interpretáveis, já que não existe uma DDD padrão em pediatria, pois as doses individuais variam de acordo com o peso da criança.
Existe um claro viés na aplicação da DDD relativo a terapia combinada com antimicrobianos: o uso de metronidazol + cefazolina para tratar uma infecção intra-abdominal, embora de espectro mais estreito, resultará no dobro de DDDs quando comparada ao uso de meropenem ou piperacilina/tazobactam isoladamente. O uso de maiores doses em gramas dos antimicrobianos para tratamento de infecções mais graves, pacientes obesos ou com infecção no sistema nervoso central podem superestimar a DDD; doses menores para ajustes de insuficiência renal, podem gerar resultados subestimados na DDD.
Enfim, dado que as doses administradas dos antimicrobianos diferem da DDD padrão definida pela OMS para vários destes, é difícil inferir os dias de terapia a partir da DDD ou construir conclusões sobre o uso relativo de um antimicrobiano comparado a outro. Nessas situações, as medidas de DOT e LOT, complementam as análises quanto ao consumo e uso de antimicrobianos40.
A medida do DOT é relativamente intuitiva e oferece maior relevância clínica e maior precisão na relação entre o tratamento recebido e o paciente, em comparação com a DDD.
Uma significativa limitação do DOT, como também da DDD, é a situação da terapia combinada de antimicrobianos versus monoterapia para a mesma indicação clínica. Num tratamento de 7 dias, dois antimicrobianos combinados contribuem para 14 DOTs, enquanto em monoterapia soma 7 DOTs. Esta discrepância pode ser corrigida pela medida de LOT. O número de antimicrobianos usados no tratamento é irrelevante na LOT, mas não na DOT.
Outra limitação dos indicadores DDD, DOT e LOT refere-se ao fato de que estes não analisam se as indicações dos antimicrobianos estão corretas.
Para as três medidas, DDD, DOT e LOT, o denominador mais frequentemente padronizado é o número de pacientes-dia ou leitos-dia e o resultado do cálculo é multiplicado e expresso por 100 ou 1.000 pacientes-dia. O valor de pacientes-dia é calculado pela soma do número de pacientes internados na unidade/setor, a cada dia, durante o período avaliado.
Outras medidas como a razão DOT/LOT, Dias Livres de Antimicrobianos (dias em que os pacientes não estão recebendo antimicrobianos), Dias de Exposição a Antimicrobianos (Antimicrobianos-dia) e a Razão de Utilização de Antimicrobianos podem ser aplicados com ganhos em complementariedade e peculiaridade de análises, entretanto, ainda carecem de maior difusão de sua aplicabilidade e validação.
D. Outros Indicadores/medidas de processo
Outras medidas de processo recomendadas incluem a distribuição proporcional das indicações para os antimicrobianos prescritos, percentual da prescrição de antimicrobianos com suspensão/revisão, percentual de revisão dos antimicrobianos prescritos após 48-72 horas do início da antibioticoterapia, percentual de descalonamento da antibioticoterapia inicial, percentual de adesão aos protocolos de antibioticoterapia empírica e de profilaxia cirúrgica e eventos redundantes de antibioticoterapia.
Taxa percentual de adequação da antibioticoterapia empírica ou antibioticoprofilaxia em cirurgia
Pode ser calculada para cada item correto da prescrição: indicação, dose, duração ou considerar todos os itens. É importante auditar a adequação com base no protocolo institucional definido.
Seguem abaixo algumas fórmulas de cálculos para esses indicadores:
Antibioticoprofilaxia cirúrgica adequada:
No de pacientes que recebeu antibioticoprofilaxia cirúrgica, de acordo com o protocolo definido pelo hospital X 100
No de procedimentos cirúrgicos realizados
Antibioticoprofilaxia cirúrgica no tempo certo:
No de pacientes que recebeu antibioticoprofilaxia cirúrgica até 1h antes do procedimento X 100
No de procedimentos cirúrgicos realizados
Antibioticoterapia empírica adequada:
No de pacientes que recebeu antibioticoterapia empírica conforme o protocolo definido pelo hospital X 100
No de pacientes com antibioticoterapia prescrita
3.1.5.2 Indicadores de resultado/desfecho
Os indicadores de resultados ou desfecho podem ser categorizados em microbiológicos, clínicos e financeiros (custos).
A. Microbiológicos: Infecção por Clostridium difficile e resistência bacteriana
Estabelecer o impacto dos programas de gerenciamento do uso de antimicrobianos sobre o desenvolvimento da resistência microbiana usando as medidas correntes tem limitações inerentes, porque vários fatores podem afetar a resistência tornando muito difícil encontrar uma associação causal clara entre as intervenções e a redução da resistência42,43.
Os principais indicadores recomendados para análise do impacto microbiológico são as taxas de incidência de infecção por C. difficile e por bactérias multirresistentes de destaque, como as enterobactérias produtoras-ESBL, as Gram-negativas (Acinetobacter spp., Pseudomonas aeruginosa e Klebsiella pneumoniae) e também as Gram-positivas (Staphylococcus aureus e Enterococcus spp.).
Infecção por Clostridium difficile
Programas que restringem o uso de clindamicina e de outras classes de antimicrobianos de risco associam-se com redução da taxa de infecção por C. difficile.
Fórmula de cálculo da Taxa de Infecção (colite) por Clostridium difficile:
Número de pacientes com colite por C. difficile X 10.000
Pacientes-dia
Resistência bacteriana
Taxa de incidência de bactérias multirresistentes selecionadas:
No de infecções pela bactéria multirresistente selecionada* X 1000 ou 10.000
Pacientes-dia
* Exemplos: Acinetobacter baumanni, Pseudomonas aeruginosa ou Klebsiella pneumoniae resistentes a carbapenêmicos, ou S. aureus resistente à oxacilina, ou Enterococcus spp resistente aos glicopeptídeos.
B. Resultados (desfechos) clínicos
Um dos objetivos primários dos programas de gerenciamento do uso de antimicrobianos é otimizar os resultados dos pacientes tratados com esses medicamentos. Desfechos sobre os resultados clínicos dos pacientes como, taxas de mortalidade global e específica relacionada a bactérias resistentes, extensão da permanência (duração da hospitalização), taxas de melhora clínica/cura e readmissão relacionada a diagnósticos infecciosos e taxas de reações adversas aos antibióticos, podem ser elementos importantes para demonstrar o impacto clínico desses programas.
C. Resultados financeiros
Indicadores de custo
Avaliações de custos sobre o consumo de antimicrobianos devem ser estimuladas e implementadas. Uma medida que pode ser utilizada é denominada Custo da Terapia (“Cost of Therapy” – COT).
A redução de custo é um importante desfecho para programas de gerenciamento de uso de antimicrobianos e relativamente fácil de mensurar. Entretanto, como os custos de aquisição de antimicrobianos podem variar institucionalmente, localmente e ao longo do tempo, não podem ser usados para propostas de mensuração do desempenho do hospital em comparação com outros serviços de saúde.
O custo com antimicrobianos pode ser calculado no hospital em geral ou em uma unidade específica em determinado período de tempo. Também pode ser medido para tratamentos específicos ou por indicação clínica.
3.1.6 Divulgação dos resultados do Programa
A documentação e a análise de dados do monitoramento são necessárias para demonstrar o impacto das atividades do Programa sobre os resultados clínicos, a resistência microbiana aos antimicrobianos e os custos de cuidados de saúde do hospital12.
Os dados sobre o uso e os custos de antimicrobianos, as susceptibilidades bacterianas a agentes antimicrobianos de antibiogramas específicos de unidades e do hospital, taxas de IRAS (infecção de sítio cirúrgico, infecção primária de corrente sanguínea, entre outras) e indicadores de qualidade relacionados à infecção devem ser comparados antes e depois da implementação do Programa e ao longo do tempo para documentar o impacto das suas atividades e identificar tendências. Além disso, os dados institucionais também podem ser comparados com os dados de outros hospitais locais e com dados de literatura publicada.
A divulgação sistemática e regular de informações sobre o resultado do Programa para todos os profissionais do hospital, com ênfase para gestores, médicos, enfermeiros e funcionários relevantes no gerenciamento do uso de antimicrobianos é um dos elementos-chave para um Programa bem-sucedido.
A divulgação pode ser feita por meio de relatórios, boletins informativos, páginas eletrônicas, painéis, entre outras formas de comunicação.
Devem ser elaborados e divulgados relatórios do Programa voltados para o time gestor e lideranças do hospital que incluam informações sobre o uso geral de antimicrobianos e as tendências, as intervenções realizadas, as atualizações sobre o progresso descrevendo as dificuldades e recomendações para melhorias futuras.
É recomendável também a divulgação de relatórios específicos para as unidades ou profissionais diretamente envolvidos com o gerenciamento do uso de antimicrobianos, por exemplo, dados de profilaxia cirúrgica para cirurgiões, tratamento de pneumonia adquirida na comunidade e infecções do trato urinário e infecções de pele para clínicos, consumo de antimicrobianos para UTI, entre outros.
Criar uma “marca” para o Programa com um slogan e logotipo pode unificar e criar reconhecimento entre funcionários do hospital para vários componentes do Programa. Esta marca pode ser aplicada a todas as comunicações (por exemplo, memorandos, cartazes, boletins informativos, correio eletrônico), formulários de pedidos e interfaces de computador usados no Programa. Uma página eletrônica interna também pode ser desenvolvida para fornecer uma fonte abrangente e conveniente de informações do Programa para a equipe do hospital.
3.2 IMPORTÂNCIA DA FARMÁCIA CLÍNICA E DA ATENÇÃO FARMACÊUTICA PARA A PRESCRIÇÃO CORRETA DE ANTIMICROBIANOS
A atuação da farmácia clínica junto ao Programa de Gerenciamento do Uso de Antimicrobianos é primordial para melhorar os resultados em saúde do paciente e os indicadores propostos no Programa. Para seu desenvolvimento, é importante a presença de um farmacêutico clínico dedicado, com formação adequada e conhecimento nessa área.
Algumas das atividades voltadas ao uso de antimicrobianos desenvolvidas pela farmácia clínica, são citadas a seguir:
Participação no desenvolvimento e atualização de protocolos de indicação e uso;
Auditoria prospectiva da prescrição após a dispensação inicial pela farmácia;
Auxílio na detecção e prevenção de interações indesejáveis tais como medicamento-medicamento, medicamento-alimento, medicamento-nutrição enteral;
Auxílio na detecção e prevenção de reações adversas e erros de medicação;
Auxílio na otimização da posologia conforme características clínicas do paciente (peso, função e hepática, hemodiálise, diálise peritoneal), agente etiológico, sítio infeccioso e características farmacocinéticas e farmacodinâmicas do medicamento;
Otimização da forma de preparo (ex.: reconstituição, diluição, forma de administração via sondas, equipo adequado, velocidade de infusão, tempo total de infusão para manutenção de estabilidade da solução, compatibilidade);
Auxílio na monitorização terapêutica e ajuste de dose, de acordo com concentração plasmática (ex.: vancomicina, aminoglicosídeos);
Auxílio no processo de descalonamento, ajuste da terapia, terapia sequencial (conversão de terapia parenteral para oral) e suspensão de tratamento;
Educação dos profissionais de saúde;
Notificação de suspeita de reação adversa a medicamentos, erro de medicação, suspeita de desvio de qualidade ou ineficácia terapêutica;
Orientação do paciente, especialmente no momento da alta.
Em situações onde não existe recursos humanos suficientes para execução de tais atividades, podem ser priorizados grupos de pacientes com maior risco de desenvolver eventos adversos (neonatos, crianças, idosos, gestantes, nefropatas, hepatopatas, ou pacientes em estado crítico), vinculando, ou não, este critério de inclusão a um perfil de uso de antimicrobianos específicos (ex.: os de uso restrito, os utilizados para bactérias multirresistentes relevantes para a instituição ou os que demandam ajuste de dose conforme concentração plasmática).
A adoção ou incorporação das atividades da farmácia clínica ao sistema informatizado da instituição torna-o mais dinâmico, padronizado e menos propenso a erros; porém, não deve substituir a análise cuidadosa e individualizada das peculiaridades de cada paciente do serviço.
3.3 IMPORTÂNCIA DOS LABORATÓRIOS DE MICROBIOLOGIA E CLÍNICO PARA A PRESCRIÇÃO CORRETA DE ANTIMICROBIANOS
O laboratório de microbiologia clínica tem papel importante para a prescrição correta de antimicrobianos pois isola, identifica e determina o perfil de sensibilidade a antimicrobianos dos patógenos causadores de infecções. Esses resultados viabilizam a reavaliação e a readequação da terapia antimicrobiana prescrita empiricamente. Além disto, os antibiogramas são utilizados na elaboração de guias terapêuticos locais pelos programas de gerenciamento do uso racional de antimicrobianos.
Tem sido discutido se o laboratório de microbiologia deveria emitir laudos de antibiogramas seletivamente (“em cascata”), ou seja, reportar a sensibilidade a antimicrobianos de amplo espectro ou mais caros somente quando houvesse resistência aos antimicrobianos de menor espectro. Porém, até o momento não há evidência que esta seja uma medida efetiva que leve definitivamente à redução do uso de antimicrobianos ou das porcentagens de resistência antimicrobiana. Dessa maneira, cada programa de gerenciamento do uso de antimicrobianos deve decidir em conjunto com a equipe do laboratório de microbiologia a respeito da implantação desta medida e, posteriormente, quanto a avaliação da adoção da mesma.
Além de auxiliar o Serviço de Controle de Infecção Hospitalar (SCIH) na investigação de surtos, os laboratórios de microbiologia devem ser responsáveis pela emissão de relatórios periódicos, onde reportem os patógenos isolados dos diferentes espécimes clínicos com seus perfis de sensibilidade e informações do paciente (iniciais, idade, data e local de internação, etc.) que permitam ao SCIH, entre outras coisas, discriminar a etiologia e o perfil de sensibilidade dos patógenos responsáveis pelas infecções comunitárias daquelas relacionadas à assistência à saúde, além de determinar a distribuição de agentes etiológicos e dos respectivos perfis de sensibilidade nas diferentes unidades de saúde ou de acordo com a faixa etária.
O emprego de testes moleculares rápidos e espectrometria de massa (MALDI-TOF) para identificação das espécies bacterianas e do perfil de sensibilidade em hemoculturas tem sido associado à diminuição do tempo para início da terapia antimicrobiana adequada, da mortalidade, do tempo de hospitalização e dos custos hospitalares. Como a implantação destes testes na rotina laboratorial necessita de recursos laboratoriais extras, como por exemplo, a aquisição de equipamentos e o funcionamento do laboratório em período integral (24h por dia nos sete dias da semana), a implantação destas medidas são sugeridas sempre que possível. Porém, elas não são mandatórias já que vários estudos mostraram que a identificação do agente etiológico foi mais rápida com o uso dessas metodologias, mas falharam em demonstrar consistentemente a redução no tempo de hospitalização ou das taxas de mortalidade. Estes resultados podem não ter sido alcançados porque, na maioria das vezes, os laboratórios não funcionavam em período integral.
Embora a confirmação do diagnóstico de infecções virais por testes rápidos auxilie na redução da prescrição de antimicrobianos, faltam estudos que confirmem o real benefício do emprego desses testes na redução do tempo de internação ou do uso de antimicrobianos.
Não podemos esquecer que os resultados dos testes microbiológicos dependem das etapas que antecedem a execução dos testes laboratoriais (fase pré-analítica). Dessa maneira, os laboratórios de microbiologia devem redigir o manual de exames microbiológicos com informações sobre coleta, transporte e armazenamento das amostras biológicas além de treinar os profissionais que atuam nessa área. As metodologias empregadas pelos laboratórios de microbiologia foram detalhadas no Manual de Microbiologia Clínica para o Controle de Infecção Relacionada à Assistência à Saúde, disponíveis no Hotsite da Anvisa: http://www20.anvisa.gov.br/segurancadopaciente/index.php/publicacoes/category/manuais.
Embora não constitua uma atividade executada diretamente pelo laboratório de microbiologia, o monitoramento dos níveis séricos de antimicrobianos também é uma das tarefas realizadas pelo laboratório que auxiliam na adequação da dose de antimicrobiano prescrita22. Outra atividade realizada pelo laboratório clínico seria o monitoramento sérico de biomarcadores. Uma meta-análise Cochrane sugere que o uso de pró-calcitonina para guiar a duração do tratamento poderia reduzir em 51% o consumo de antibióticos em pacientes hospitalizados com infecções bacterianas em diversos sítios anatômicos. Os níveis de pró-calcitonina refletem a replicação bacteriana e foram amplamente testados para orientar as decisões de quando usar ou interromper o uso de antibióticos. Uma meta-análise de 7 ensaios clínicos randomizados com 1458 pacientes mostrou que as decisões guiadas por pró-calcitonina reduziram o uso total de antibióticos em 51% sem alterar o desfecho.
A parceria forte entre os laboratórios microbiológico e clínico e o Programa de Gerenciamento do Uso de Antimicrobianos resulta na melhoria da qualidade da assistência oferecida ao paciente e maior chance de sucesso terapêutico.
3.4 AÇÕES PARA PROMOÇÃO DO USO CORRETO DE ANTIMICROBIANOS EM SERVIÇOS DE ATENÇÃO BÁSICA
De acordo com a Política Nacional de Atenção Básica (PNAB), publicada pela Portaria nº 2.436, de 21 de setembro de 201746, que estabelece a revisão de diretrizes para a organização da Atenção Básica, no âmbito do Sistema Único de Saúde (SUS), a Atenção Básica “é o conjunto de ações de saúde individuais, familiares e coletivas que envolvem promoção, prevenção, proteção, diagnóstico, tratamento, reabilitação, redução de danos, cuidados paliativos e vigilância em saúde, desenvolvida por meio de práticas de cuidado integrado e gestão qualificada, realizada com equipe multiprofissional e dirigida à população em território definido, sobre as quais as equipes assumem responsabilidade sanitária”.
Apesar da prevalência de colonização e infecções causadas por microrganismos multirresistentes ser atualmente mais documentada nos hospitais, a maior parte das prescrições de antimicrobianos é feita fora deles, em especial nos serviços de atenção básica, como as Unidades Básicas de Saúde (UBS), e o maior consumo desses medicamentos ocorre na comunidade em geral.
A prescrição de antimicrobianos em serviços como as UBS tem sido uma preocupação, especialmente pela dificuldade em garantir a sua utilização correta (dose e duração do tratamento) pelos pacientes.
Desta maneira, é fundamental a implementação de ações de promoção do uso correto de antimicrobianos na atenção básica, como por exemplo:
Elaboração e implantação de protocolos para diagnóstico e tratamento das infecções mais prevalentes;
Educação dos profissionais da saúde;
Educação dos pacientes/familiares/cuidadores.
3.4.1 Elaboração e implantação de protocolos para diagnóstico e tratamento das infecções mais prevalentes
Os protocolos são diretrizes embasadas em evidências científicas e práticas de consensos, cuja implantação demonstrou ser efetiva e fundamental para promover o uso correto de antimicrobianos, padronizando as condutas e prescrição, sendo uma estratégia efetiva adotada em diversos países e em todos os níveis de atenção, desde a atenção básica até os serviços mais complexos.
É imprescindível nos serviços de atenção básica a adoção de protocolos para manejo das patologias mais comumente atendidas. Tais protocolos podem ser criados ou adaptados de protocolos já existentes. Sua divulgação e a realização de treinamentos voltados para os profissionais de saúde, principalmente para os prescritores, são fundamentais para sua implantação e para se atingir os objetivos propostos.
Os protocolos auxiliam os profissionais na tomada de decisão em relação à estratégia de diagnóstico e da alternativa terapêutica mais adequada, e devem incluir, no mínimo, sugestões para o diagnóstico e opções de antimicrobianos para o manejo das infecções mais prevalentes na comunidade, tais como:
• Dermatites bacterianas e infecções de pele e partes moles;
• Gastroenterites bacterianas;
• Infecção do trato urinário;
• Infecções sexualmente transmissíveis (IST);
• Otite, sinusite, faringoamigdalite;
• Pneumonia.
Para medicamentos administrados na própria unidade de saúde, o protocolo deve contemplar a forma de preparo (ex.: diluente compatível e volume para reconstituição de pó liofilizado e diluição para infusão) e administração (ex.: via, velocidade de infusão).
Alguns tópicos importantes para a elaboração de protocolos de diagnóstico e tratamento são:
• definir o assunto e objetivos do protocolo que será desenvolvido;
• designar uma equipe multiprofissional para elaboração, especificando suas atribuições;
• realizar a pesquisa bibliográfica sobre os tópicos incluídos no protocolo;
• identificar as evidências que o fundamentam, citando sua fonte;
• estabelecer sua periodicidade de revisão e atualização.
Os protocolos de tratamento das principais infecções em atenção básica do Ministério da Saúde podem ser utilizados para consulta ou adaptação à realidade local.
Para implantação dos protocolos são recomendadas, no mínimo, as seguintes ações:
• Determinação de fluxos padronizados e de fácil entendimento para a prescrição, a dispensação e a administração, quando se tratar de antimicrobiano administrado na unidade de saúde;
• Educação e treinamento de todos os profissionais da saúde quanto à disponibilidade e necessidade de adoção dos protocolos desenvolvidos;
• Facilitação do acesso aos protocolos, disponibilizando os mesmos em versão impressa e/ou eletrônica em locais acessíveis.
3.4.2 Educação dos profissionais da saúde
A educação permanente dos profissionais de saúde visa aumentar a conscientização sobre a importância da prescrição dos antimicrobianos, seguindo os protocolos definidos localmente, com o objetivo de garantir o efeito fármaco-terapêutico máximo dos antimicrobianos, reduzindo a ocorrência de eventos adversos nos pacientes atendidos e prevenindo a seleção e a disseminação de microrganismos multirresistentes.
Como medidas educativas, além de capacitações presenciais ou à distância, seminários e treinamentos para todos os profissionais de saúde do serviço, podem ser disponibilizados guias de orientação sobre medidas de prevenção de infecção e uso terapêutico de antimicrobianos.
É também imprescindível que os prescritores sejam treinados e que atendam às boas práticas de prescrição de antimicrobianos descritas no Anexo I. As orientações desse Anexo devem ser adaptadas à realidade do serviço de atenção básica. A seguir, exemplificamos alguns pontos relevantes das boas práticas de prescrição que devem ser considerados nos serviços de atenção básica:
Ao definir a posologia, considerar a comodidade de uso pelo paciente para aumentar a adesão ao tratamento (dar preferência por medicações de dose única diária ou de 12/12 horas);
Infecções mais graves, com dificuldade de adesão do paciente ou situações emergenciais, podem demandar administração por via parenteral no início ou durante toda a duração do tratamento e assim, o paciente deverá ser encaminhado para uma unidade de saúde de maior complexidade;
Ao prescrever a medicação, se houver necessidade de diluição, é fundamental que o paciente seja orientado a seguir o que está previsto na bula do medicamento.
3.4.3 Educação dos pacientes/familiares/cuidadores
Quando pacientes, familiares ou cuidadores são os responsáveis pela administração do medicamento, a educação é primordial e deve ser feita, quando possível, diretamente a eles, com linguagem adequada à sua realidade, devendo contemplar:
Forma de preparo e armazenamento (ex.: diluente para soluções orais, necessidade de refrigeração);
Posologia (ex.: horários de administração, tempo de uso) destacando a necessidade de seguir com o tratamento mesmo após melhora nos sinais e sintomas;
Forma de uso (ex.: administração com água, em jejum ou durante as refeições);
Interações medicamento-medicamento, medicamento-alimento;
Procedimento em caso de esquecimento de dose;
Principais reações adversas associadas ao uso do antimicrobiano e como proceder caso ocorram;
Modo de descarte (não descartar na pia ou vaso sanitário ou no lixo comum, por exemplo);
Não utilização de sobras de tratamentos anteriores (pelo próprio paciente ou outros familiares/vizinhos etc.)
Todos os profissionais de saúde devem estar envolvidos no processo de educação do paciente, familiares e cuidadores. A orientação da equipe multiprofissional é imprescindível para a correta administração do antimicrobiano, quanto aos horários, modo de usar, tempo de tratamento, possíveis interações medicamentosas, efeitos adversos previstos e consequente adesão ao tratamento.
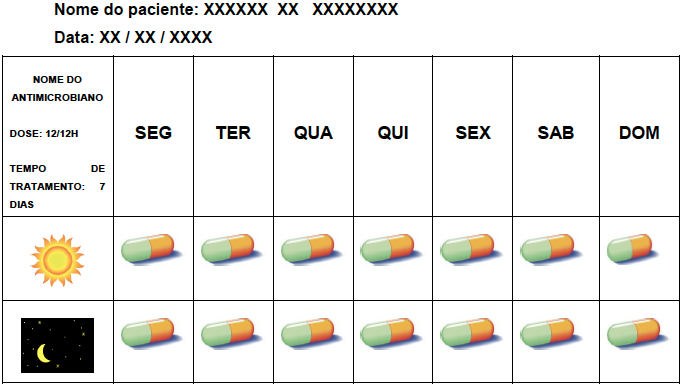
Para evitar falhas terapêuticas devido ao uso inadequado da medicação por dificuldade de leitura e interpretação do paciente, pode ser necessário o uso 48
de tabelas com desenhos e cores para facilitar o entendimento da prescrição (posologia, duração do tratamento, horários da medicação). Segue abaixo um exemplo de tabela que pode ser elaborada: